|
NOVIDADES
Nanopartículas sintéticas de HDL carregadas com RNA de interferência para silenciar genes promotores do câncer são seletivas para diminuir câncer de ovário em ratos. A descoberta foi realizada pela equipe de pesquisa liderada por cientistas do MD Anderson Cancer Center da Universidade do Texas e do Health Science Center da Universidade do Texas Norte e foi publicada na edição de abril, da revista Neoplasia. "RNA de Interferência tem grande potencial terapêutico, mas levá-lo às células cancerosas tem sido problemático", disse o médico Anil Sood, autor sênior do estudo, diretor do Ovarian Cancer Research e vice-diretor do Center for RNA Interference and Non-Coding RNA do MD Anderson. "Combinar siRNA e HDL é uma maneira eficiente para levar estas moléculas até seus alvos. Este estudo tem várias implicações importantes quanto a capacidade de combater certos tipos de câncer." 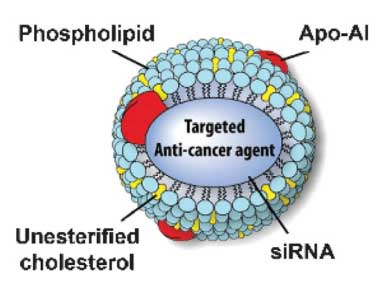 Créditos: Neoplasia.
O próximo passo é se preparar para testes clínicos em humanos, afirmam os dois cientistas. "Se foi possível combater 70, 80 ou 90% dos tumores em camundongos, sem acúmulo do fármaco nos tecidos normais, é provável que muitos pacientes com câncer poderão se beneficiar deste novo tipo de tratamento a longo prazo", disse Lacko. Tentativas anteriores para entregar siRNA usando lipossomas e outras nanopartículas têm encontrado barreiras devido à toxicidade e outros aspectos concernentes. Por exemplo, os minúsculos fragmentos de RNA, que regulam genes de forma altamente seletiva, simplesmente não podem ser injetados. "Se o siRNA não é uma nanopartícula, ele se quebra e é excretado antes de exercer sua função", disse Sood. "HDL é completamente biocompatível e é uma melhoria segura quando comparado com outros tipos de nanopartículas". A equipe desenvolveu uma versão sintética de HDL, chamada rHDL, porque é mais estável que a versão natural. Os investigadores primeiro confirmaram a distribuição de SR-B1 e a absorção de nanopartículas de rHDL injetadas em camundongos com células cancerosas. Descobriram que o siRNA foi distribuído uniformemente em cerca de 80 por cento do tumor tratado. Como esperado, as nanopartículas se acumularam no fígado, com entrega mínima ou nenhuma no cérebro, coração, pulmão, rim ou baço. Os estudos de segurança mostraram que a absorção no fígado não causa efeitos adversos. Usando siRNA específicos a um gene individual, os pesquisadores separadamente silenciaram os genes STAT3 e FAK em vários tipos de tumores resistentes ao tratamento do câncer de ovário. STAT3 e FAK são importantes para o crescimento do câncer, progressão e metástase, não obstante também desempenham papel importante no tecido normal, de modo que a precisão em alvejar precisamente o tumor é vital. A formulação siRNA/rHDL sozinha reduziu o tamanho e o número de tumores em 60 a 80 por cento. Combinações com quimioterapia causaram reduções acima de 90 por cento. As abordagens convencionais para alvejar o STAT3 tiveram sucesso limitado, disse Sood. O FAK, que é mais expresso em cânceres colorretal, tireóide, mama, ovário e próstata, é particularmente agressivo no câncer de ovário e uma das razões para o baixo tempo de sobrevida. Tentativas anteriores alvejaram o FAK com nanopartículas de lipossomas ou pequenas moléculas inibidoras, porém estes métodos não são específicos para cada tumor e são mais propensos a prejudicar as células normais, dizem os cientistas. MD Anderson e UNT solicitaram uma patente para o método de entrega de nanopartículas.. MD Anderson Cancer Center - The University of Texas (Tradução - AGS). Nota do Scientific Editor: o trabalho que deu origem a esta notícia: "Targeted Delivery of Small Interfering RNA Using Reconstituted High-Density Lipoprotein Nanoparticles", de autoria de Mian M.K. Shahzad, Lingegowda S. Mangala, Hee Dong Han, Chunhua Lu, Justin Bottsford-Miller, Masato Nishimura, Edna M. Mora, Jeong-Won Lee, Rebecca L. Stone, Chad V. Pecot, Duangmani Thanapprapasr, Ju-Won Roh, Puja Gaur, Maya P. Nair, Yun-Yong Park, Nirupama Sabnis, Michael T. Deavers, Ju-Seog Lee, Lee M. Ellis, Gabriel Lopez-Berestein, Walter J. McConathy, Laszlo Prokai, Andras G. Lacko e Anil K. Sood, foi publicado na revista Neoplasia, Vol. 13, Número 4, págs. 309-319 (2011) e pode ser acessado em: http://dx.doi.org/ 10.1593/neo.101372. |
|||||||||||||||||||||||||